Edificio Shuangyang, ciudad de Yangshe, ciudad de Zhangjiagang, provincia de Jiangsu, China.
Edificio Shuangyang, ciudad de Yangshe, ciudad de Zhangjiagang, provincia de Jiangsu, China.
Selección Estratégica de KOL Adaptada a las Realidades Clínicas de la Traumatología Maxilofacial Priorizando Cirujanos Maxilofaciales y Médicos Especialistas en Trauma con Alta Carga Clínica según Volumen Clínico e Influencia en Protocolos Involucrar a líderes de opinión clave en traumatología maxilofacial...
VER MÁS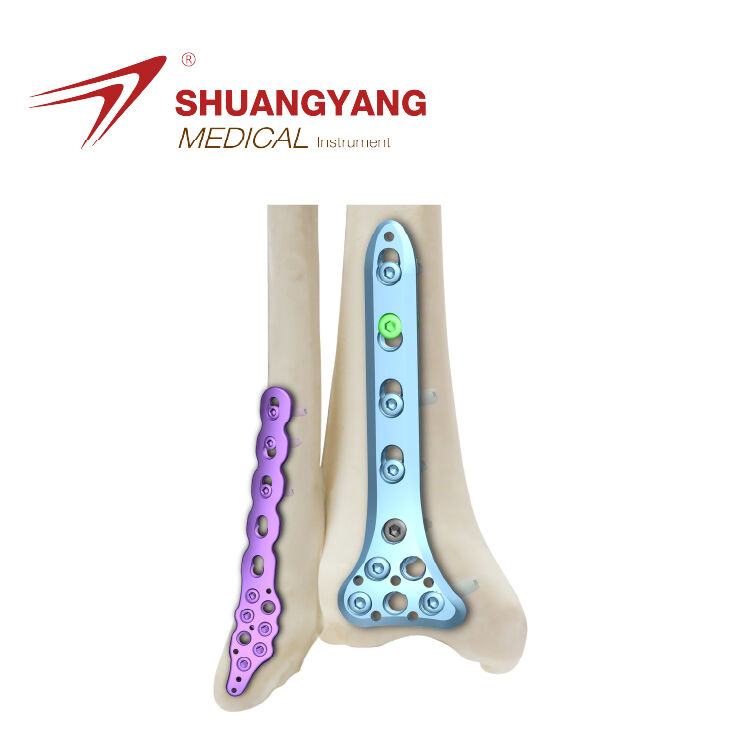
Definir Criterios Clave de Comparación para Placas de Húmero Distal Ajuste Anatómico y Precisión del Diseño Preformado Conseguir la forma correcta es muy importante al fijar fracturas en la parte inferior del hueso del brazo superior. Las placas quirúrgicas deben coincidir con la forma...
VER MÁS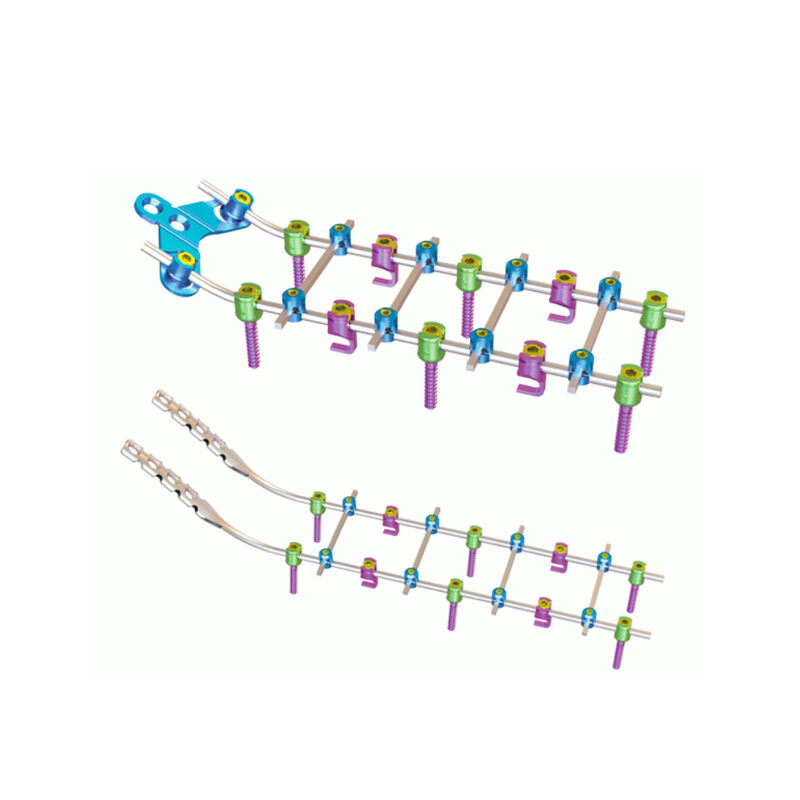
El papel de control de las políticas de reembolso en la adopción de la fusión espinal. La forma en que fluye el dinero a través del sistema sanitario actúa como el punto principal de control para determinar cuán ampliamente se utiliza la fusión espinal en los centros médicos estadounidenses. Las compañías de seguros y los gobiernos...
VER MÁS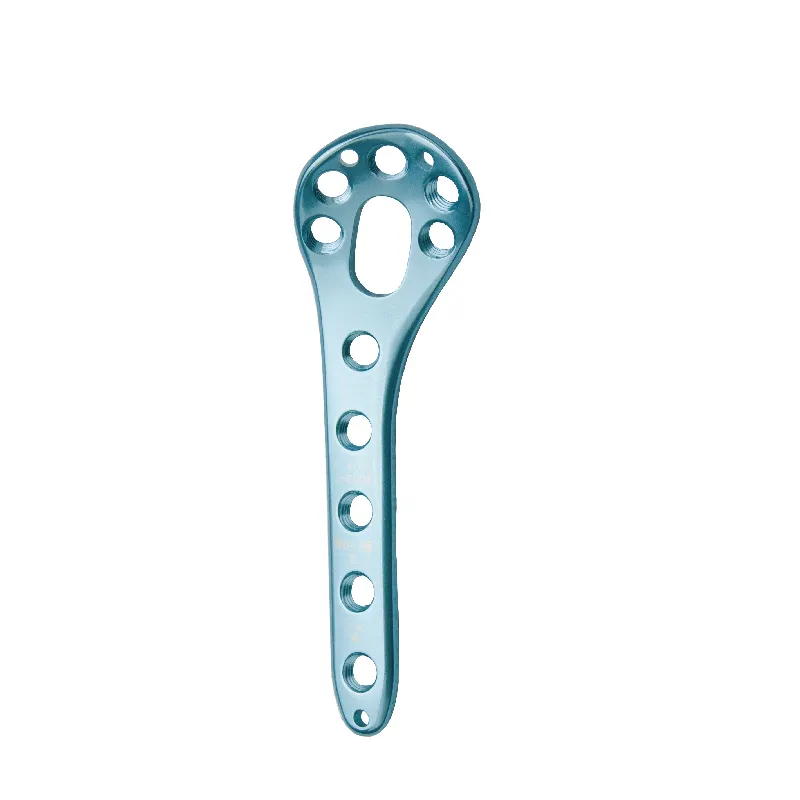
Comprensión de las necesidades clínicas insatisfechas en ortopedia pediátrica. Prevalencia y consecuencias de la deformidad de extremidades no tratada, escoliosis de inicio temprano y traumatismos pediátricos. Más de dos tercios de los problemas ortopédicos pediátricos, como las deformidades de extremidades y la escoliosis de inicio temprano...
VER MÁS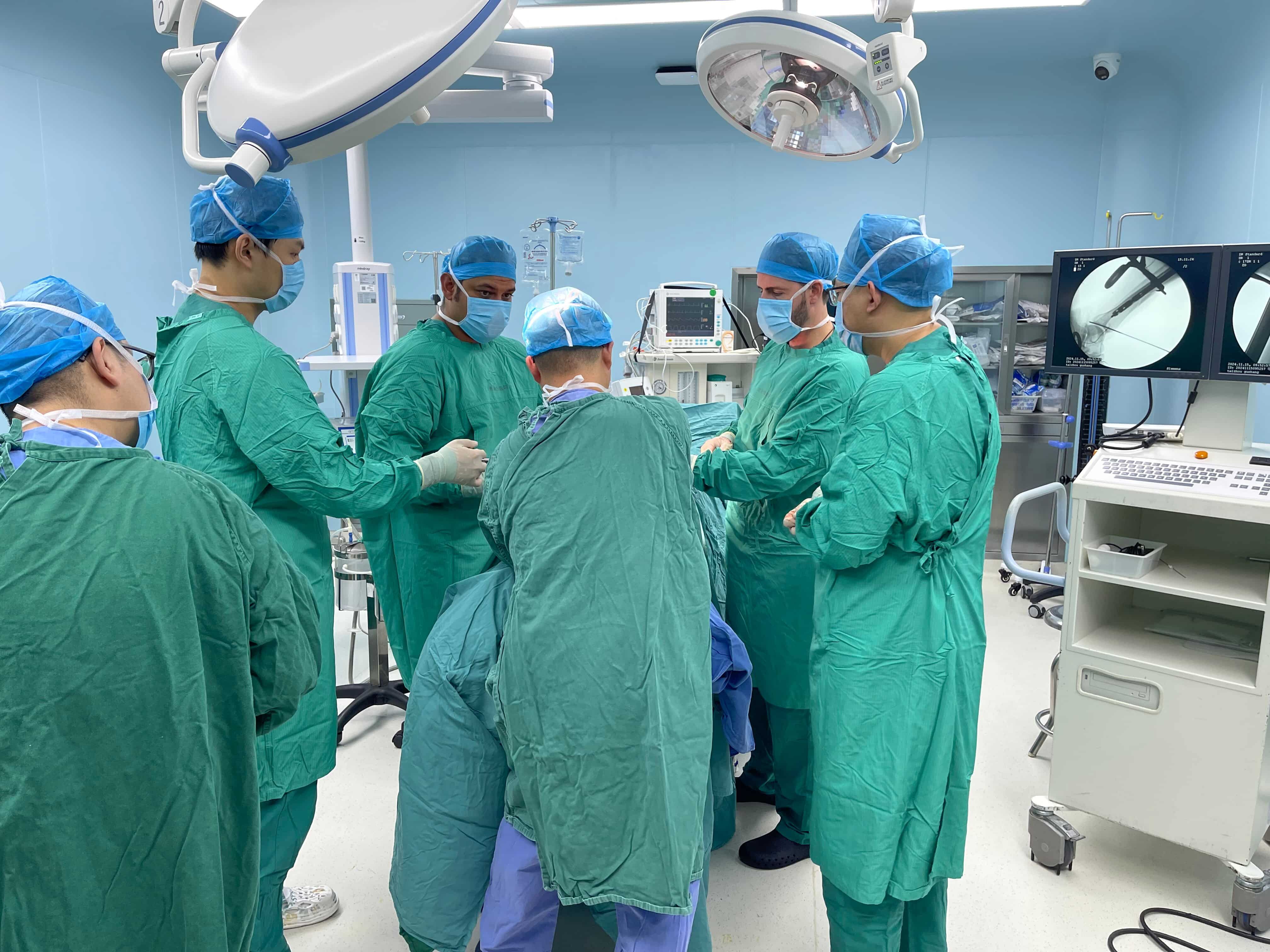
Trayectorias regulatorias y bases para el acceso al mercado Requisitos de la FDA, CE Mark y NMPA para dispositivos espinales mínimamente invasivos Superar el laberinto regulatorio representa el primer obstáculo al llevar dispositivos médicos al mercado. Para productos que entran...
VER MÁS
Por qué los mercados emergentes se están convirtiendo en un factor clave para la adopción de placas de fíbula Aumento de la carga de traumatismos ortopédicos impulsada por lesiones de tráfico y poblaciones envejecidas La demanda de soluciones con placas de fíbula sigue creciendo en mercados emergentes debido a dos factores principales...
VER MÁS
Fragilidad y funcionalidad: por qué las placas orbitales exigen un envío preciso. La integridad microestructural como imperativo clínico. Es absolutamente necesario tener cuidado especial durante el envío de las placas orbitales, ya que pequeñas imperfecciones pueden afectar significativamente la evolución del paciente después...
VER MÁS
ISO 11607: La norma principal para sistemas de barrera estéril. Parte 1: Diseño, selección de materiales y compatibilidad con el proceso de esterilización. Al elegir materiales para sistemas de barrera estéril, es necesario considerar minuciosamente la compatibilidad con diferentes técnicas de esterilización...
VER MÁS
Fallos en la Barrera Estéril: La Causa Principal de los Retiros de Dispositivos Médicos por Empaquetado. Deterioro de la Integridad del Sello y Pérdida de Esterilidad en Bolsas de Implantes. Los sistemas de barrera estéril actúan como última línea de defensa contra la contaminación para dispositivos médicos importantes...
VER MÁS
Fundamentos de Seguridad en RM para Implantes Anteriores de Columna Cervical. Descodificación del estándar ASTM F2503: Clasificaciones de Condicional, Seguro y No Seguro para Resonancia Magnética. Cuando se trata de seguridad en RM para implantes anteriores de columna cervical, todo comienza con el estándar ASTM F2503...
VER MÁS
Por qué un nivel de seguridad de esterilidad de 10^-6 es obligatorio para implantes espinales. El nivel de seguridad de esterilidad, o SAL, básicamente nos indica la probabilidad de que microorganismos vivos sobrevivan después de la esterilización. Cuando hablamos de implantes espinales espec...
VER MÁS
Por qué la extensión de la vida útil es crítica para los sistemas de sujeción con cable de titanio. Con el tiempo, los materiales tienden a degradarse, lo que crea problemas reales para los sistemas de sujeción con cable de titanio presentes en implantes médicos. Claro, las aleaciones de titanio son bastante buenas...
VER MÁS