Edificio Shuangyang, ciudad de Yangshe, ciudad de Zhangjiagang, provincia de Jiangsu, China.
Edificio Shuangyang, ciudad de Yangshe, ciudad de Zhangjiagang, provincia de Jiangsu, China.
Divergencia regulatoria: Reglamento de Dispositivos Médicos de la UE frente a los marcos de la FDA Requisitos de evidencia clínica: Vigilancia posterior a la comercialización frente a vías de autorización previa a la comercialización (PMA) Bajo el Reglamento de Dispositivos Médicos de la UE, los fabricantes deben seguir evaluando clínicamente sus productos durante todo el ciclo de vida del dispositivo...
VER MÁS
Mallas antibióticas basadas en polímeros: mecanismos e impacto clínico Cómo los recubrimientos de liberación sostenida permiten una actividad antimicrobiana localizada y de larga duración Las mallas que liberan antibióticos, fabricadas con polímeros, funcionan mediante la aplicación de recubrimientos especiales que liberan lentamente...
VER MÁS
Aproveche la Designación de Dispositivo Innovador de la FDA para acelerar la autorización regulatoria. Inscripción estratégica en el Programa de Dispositivos Innovadores de la FDA para sistemas de fijación de costillas. El Programa de Dispositivos Innovadores de la FDA, comúnmente conocido como BDP, brinda a las empresas...
VER MÁS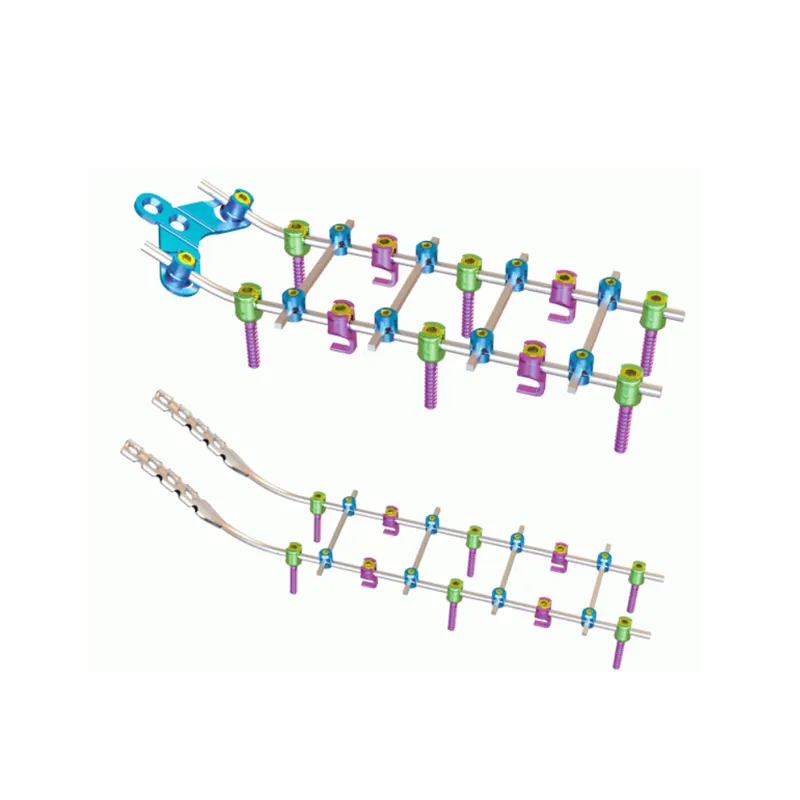
Fabricación aditiva: impulsa la personalización y la optimización biomecánica. Cages de titanio poroso fabricados mediante impresión 3D para una osteointegración mejorada y un ajuste anatómico óptimo. Con la fabricación aditiva, los cirujanos ahora pueden crear cages espinales adaptados específicamente a...
VER MÁS
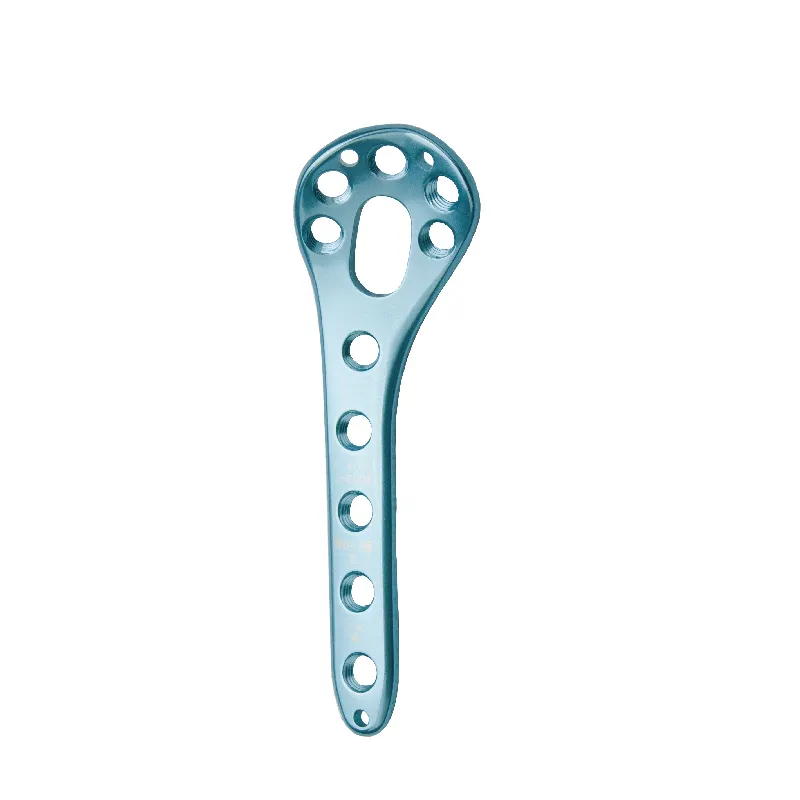
Comprensión de los requisitos para las pruebas de equivalencia de placas proximales laterales de la tibia. Por qué la identidad estructural por sí sola no garantiza la validación de la equivalencia clínica. El simple hecho de que dos placas tengan exactamente las mismas dimensiones y la misma disposición de los orificios para tornillos no significa que funcionarán de forma equivalente en la práctica clínica...
VER MÁS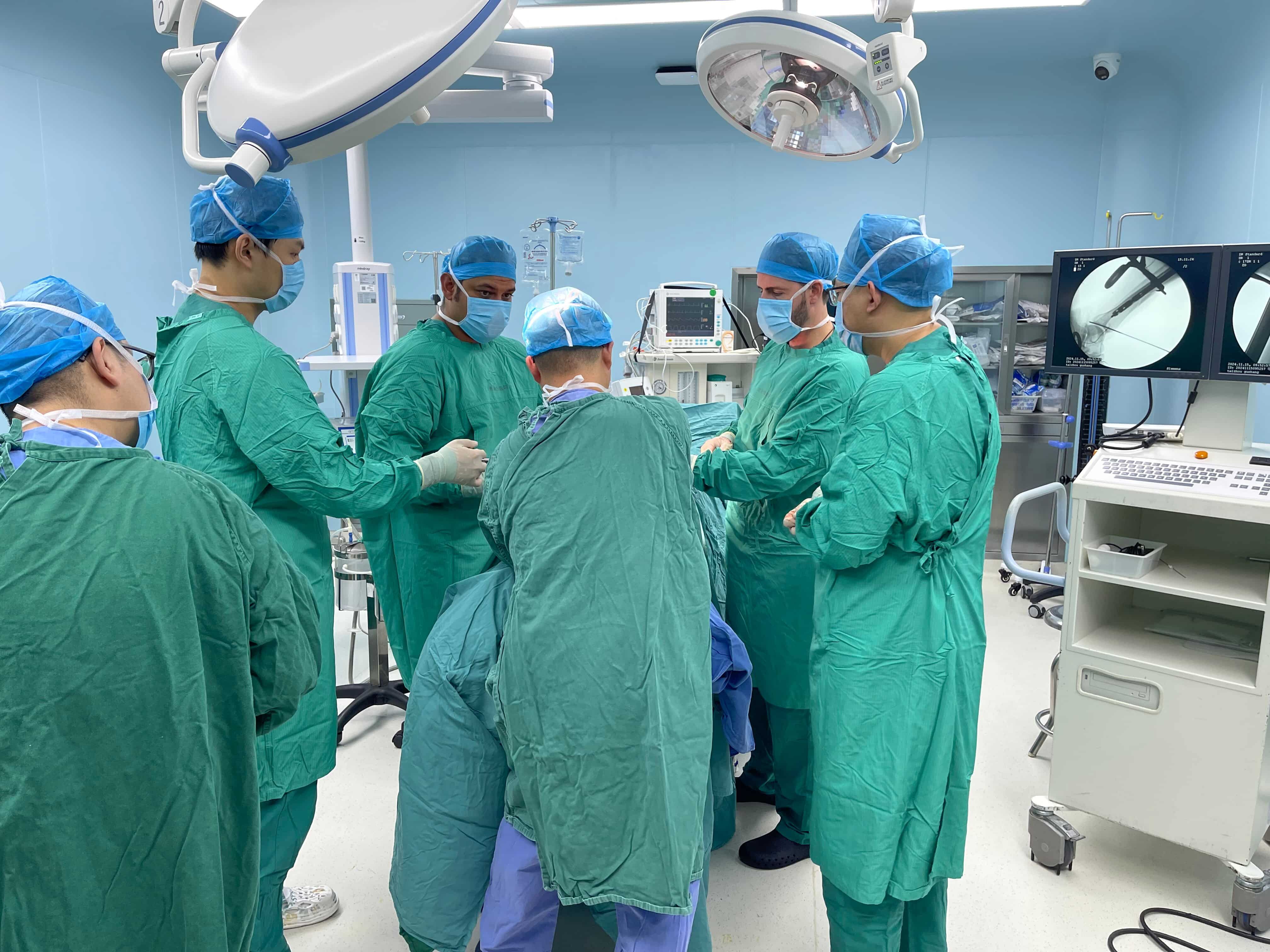
La necesidad clínica y operativa de los acuerdos de nivel de servicio (ANS) para instrumentos quirúrgicos ortopédicos. Dependencias del flujo de trabajo OR: cómo la disponibilidad de los instrumentos afecta directamente el cumplimiento del horario programado para el primer caso y la utilización de los bloques quirúrgicos. Tener listos los instrumentos quirúrgicos adecuados a tiempo es absolutamente...
VER MÁS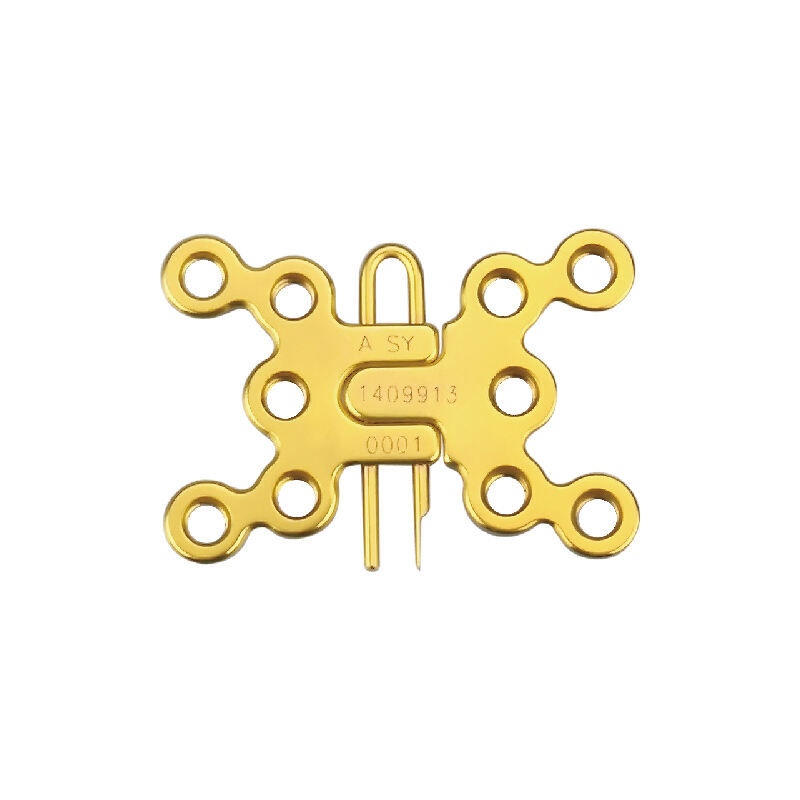
Gestión de reclamaciones por malfunciones de implantes esternales: cumplimiento normativo y flujo de trabajo. Requisitos de la FDA sobre notificación de incidentes médicos (MDR) para implantes esternales: plazos de notificación y normas de documentación. En lo que respecta a los problemas derivados de implantes esternales, los fabricantes de dispositivos médicos no tienen...
VER MÁS
Requisitos de notificación según la Ley Sunshine en ortopedia especializada. ¿Qué deben divulgar los fabricantes de dispositivos ortopédicos bajo la Ley Sunshine? Los fabricantes de dispositivos en el ámbito ortopédico deben registrar y notificar todos los pagos o transferencias de valor superiores a 1 USD que realicen...
VER MÁS
¿Por qué las devoluciones y los juegos de instrumentos prestados para pie y tobillo requieren una gestión especializada? Las cirugías ortopédicas de pie y tobillo requieren un número increíble de instrumentos —a veces más de 50 herramientas diferentes por intervención—, lo que genera todo tipo de desafíos logísticos...
VER MÁS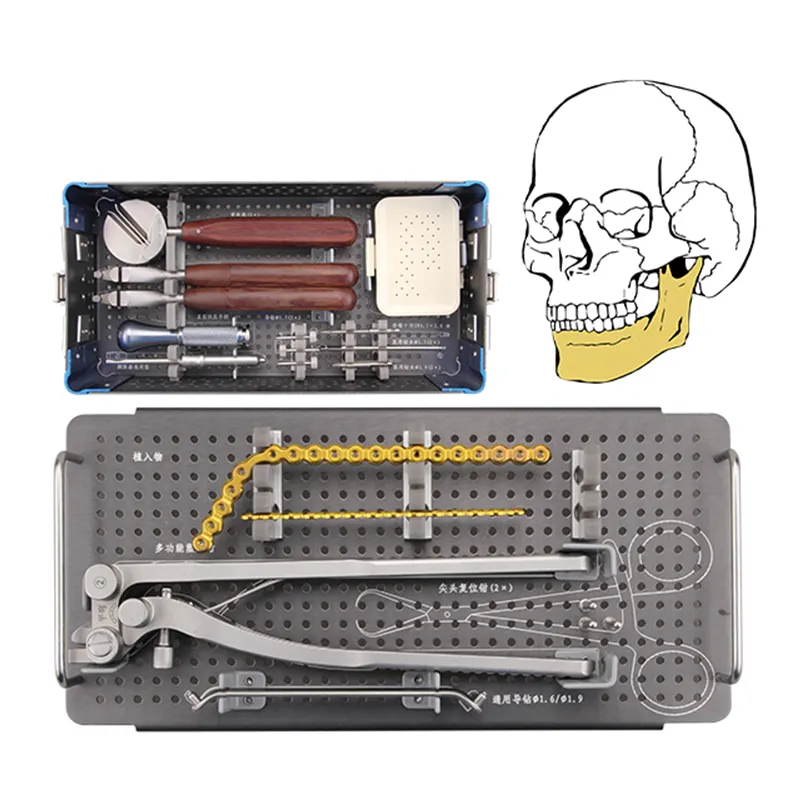
Negociación estratégica de acuerdos con distribuidores para la venta global de productos maxilofaciales: equilibrar la exclusividad, el alcance territorial y el acceso al mercado en la distribución de dispositivos CMF. Lograr acuerdos óptimos con distribuidores para la comercialización mundial de productos maxilofaciales implica...
VER MÁS
Identificar y clasificar los secretos comerciales fundamentales en la co-desarrollo de malla de titanio Distinguir la propiedad intelectual (PI) específica de la malla de titanio del conocimiento generalizado de la industria Para mantener segura la propiedad intelectual específica, las empresas necesitan una buena documentación que demuestre claramente qué es realmente...
VER MÁS
Cumplimiento normativo y mitigación de riesgos mediante la integración multifuncional temprana Cómo las transferencias fragmentadas entre departamentos retrasan la transferencia del diseño —y aumentan el riesgo de revisión por parte de la FDA Cuando I+D, fabricación y departamentos normativos trabajan de forma aislada, se generan problemas serios...
VER MÁS