Bâtiment Shuangyang, ville de Yangshe, ville de Zhangjiagang, province du Jiangsu, Chine.
Bâtiment Shuangyang, ville de Yangshe, ville de Zhangjiagang, province du Jiangsu, Chine.
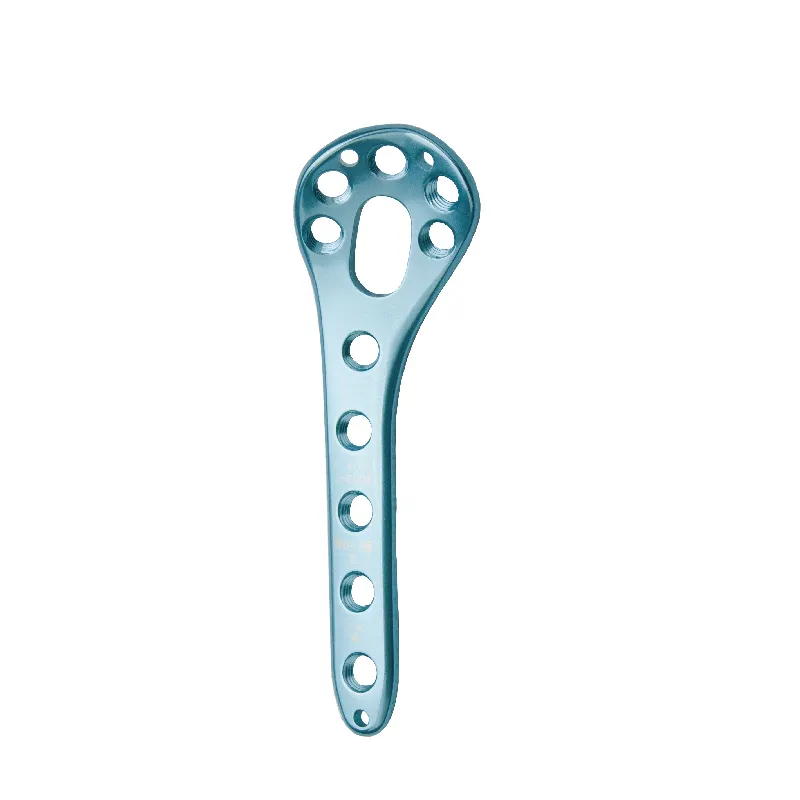
Divergence réglementaire : Règlement européen relatif aux dispositifs médicaux (MDR) contre cadre réglementaire de la FDA Exigences en matière de preuves cliniques : surveillance après mise sur le marché contre procédure d'autorisation préalable à la commercialisation (PMA) En vertu du règlement européen relatif aux dispositifs médicaux, les fabricants doivent évaluer continuellement leurs produits sur le plan clinique tout au long de leur cycle de vie complet...
VOIR PLUS
Mailles polymères libérant des antibiotiques : mécanismes et impact clinique Comment les revêtements à libération prolongée permettent une activité antimicrobienne localisée et à long terme Les mailles libérant des antibiotiques, fabriquées à partir de polymères, fonctionnent grâce à des revêtements spécifiques qui libèrent progressivement...
VOIR PLUS
Profiter de la désignation « dispositif innovant » de la FDA pour accélérer l'autorisation réglementaire. Inscription stratégique au programme « dispositif innovant » de la FDA pour les systèmes de plaquage des côtes. Le programme « dispositif innovant » (BDP) de la FDA offre aux entreprises...
VOIR PLUS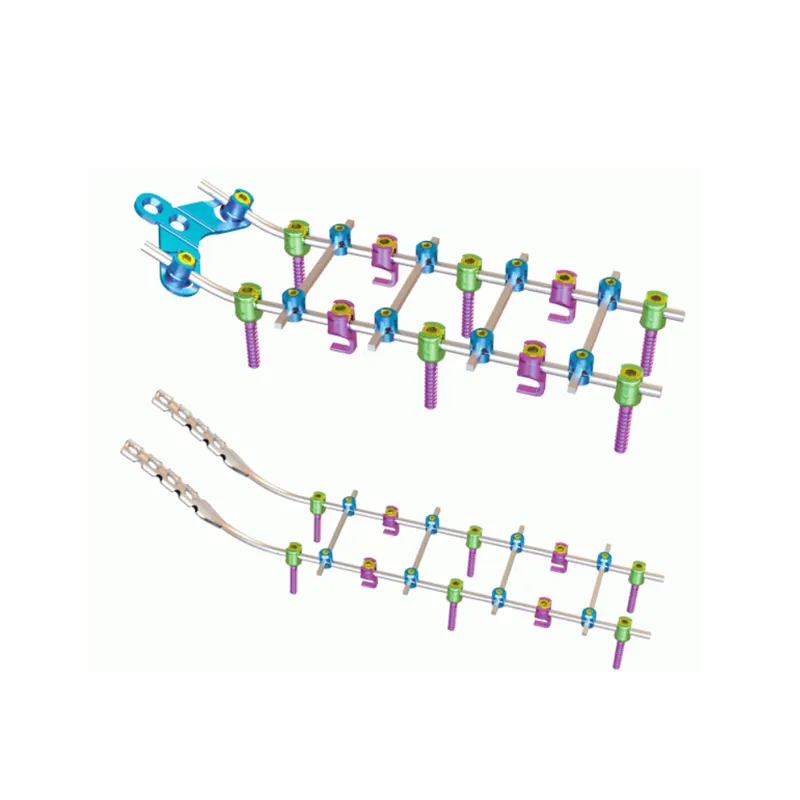
Fabrication additive : un levier de personnalisation et d'optimisation biomécanique. Cages en titane poreux fabriquées par impression 3D pour une ostéo-intégration améliorée et un ajustement anatomique optimal. Grâce à la fabrication additive, les chirurgiens peuvent désormais concevoir des cages rachidiennes spécifiquement adaptées à...
VOIR PLUS
Comprendre les exigences en matière d’essai d’équivalence pour les plaques de la partie proximale et latérale du tibia — Pourquoi l’identité structurelle à elle seule ne suffit pas pour valider l’équivalence clinique : Le fait que deux plaques aient exactement les mêmes dimensions et le même agencement des trous pour les vis ne signifie pas nécessairement qu’elles per...
VOIR PLUS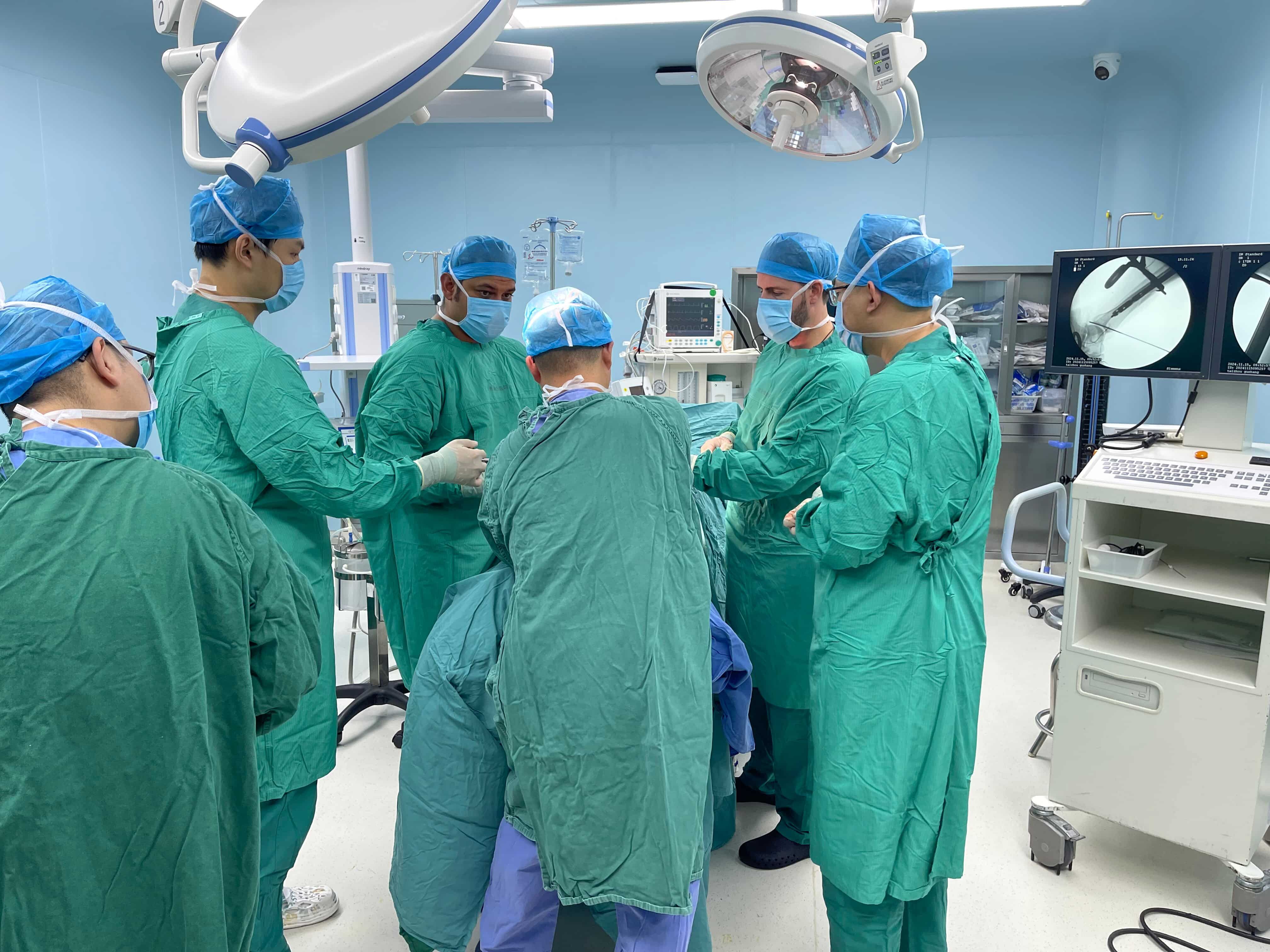
La nécessité clinique et opérationnelle des SLA pour les instruments chirurgicaux orthopédiques — Dépendances au sein des flux de travail OR : comment la disponibilité des instruments influence directement le respect de l’horaire du premier cas et l’utilisation des blocs chirurgicaux — Disposer, dans les délais impartis, des bons instruments chirurgicaux est absolument...
VOIR PLUS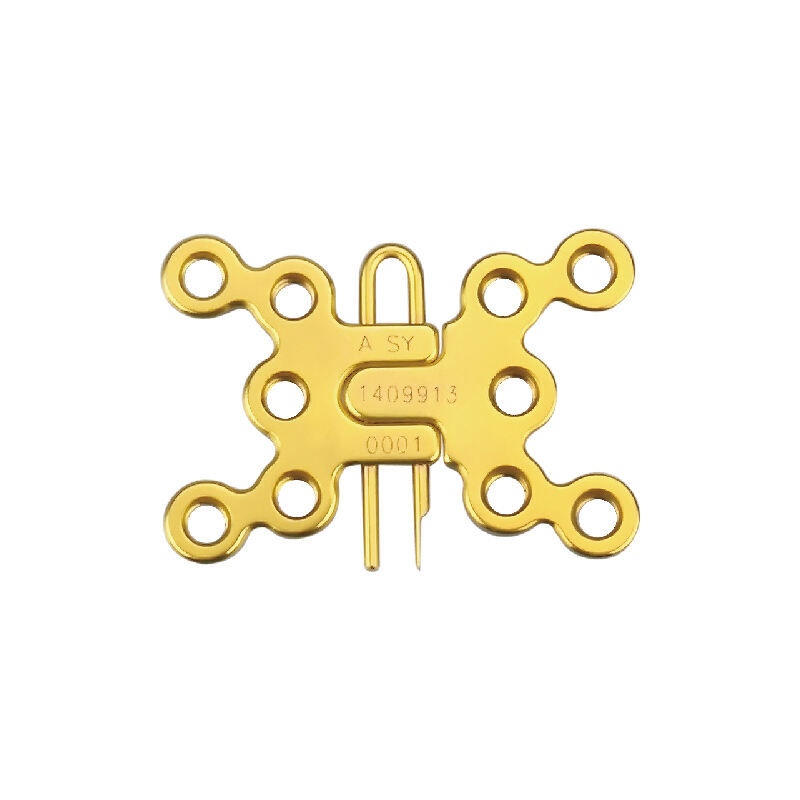
Traitement des réclamations relatives aux dysfonctionnements des implants du sternum : conformité réglementaire et flux de travail. Exigences de la FDA en matière de déclaration d’incidents (MDR) pour les implants du sternum : délais de déclaration et normes de documentation. En ce qui concerne les problèmes liés aux implants du sternum, les fabricants de dispositifs médicaux n’ont aucun...
VOIR PLUS
Exigences de déclaration au titre de la loi Sunshine dans le domaine de l’orthopédie spécialisée. Que doivent divulguer les fabricants de dispositifs orthopédiques en vertu de la loi Sunshine ? Les fabricants de dispositifs dans le domaine de l’orthopédie doivent suivre et déclarer tout paiement ou toute transmission de valeur supérieure à 1 $ qu’ils accordent...
VOIR PLUS
Pourquoi les retours et les jeux d’instruments de prêt pour le pied et la cheville exigent-ils une gestion spécialisée ? Les chirurgies orthopédiques du pied et de la cheville nécessitent un nombre impressionnant d’instruments – parfois plus de 50 outils différents par intervention – ce qui génère toute une série de défis logistiques...
VOIR PLUS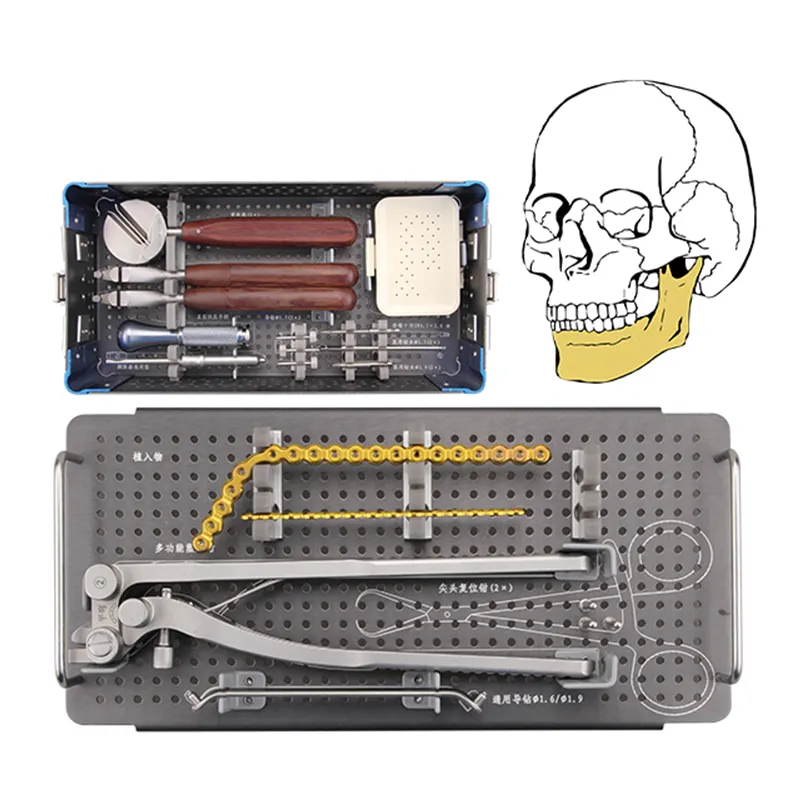
Négociation stratégique des accords de distribution pour les ventes mondiales d’implants crânio-maxillo-faciaux (CMF) : concilier exclusivité, périmètre territorial et accès aux marchés dans la distribution d’appareils CMF. Conclure des accords de distribution avantageux pour la commercialisation mondiale de produits crânio-maxillo-faciaux implique...
VOIR PLUS
Identifier et classer les secrets commerciaux essentiels dans le cadre du co-développement de mailles de titane Distinction entre la propriété intellectuelle spécifique aux mailles de titane et les savoir-faire standards du secteur Pour préserver la propriété intellectuelle spécifique, les entreprises doivent disposer d'une documentation rigoureuse attestant clairement de ce qui constitue réellement...
VOIR PLUS
Conformité réglementaire et atténuation des risques grâce à une intégration transversale précoce Comment les transferts cloisonnés retardent le transfert de conception — et augmentent le risque d’examen par la FDA Lorsque les départements R&D, fabrication et réglementaire travaillent de façon isolée, cela crée des...
VOIR PLUS